L’anémie est définie par une diminution du nombre de globules rouges ou de l’hémoglobine, mais, chez le cheval, elle résulte très rarement d’un manque de fer. Pourtant, beaucoup associent spontanément anémie et carence en fer.
Le fer étant un composant essentiel de l’hémoglobine, il paraît logique de relier les deux. Mais en réalité, l’anémie n’est qu’un signe biologique, pas un diagnostic. La confondre avec une carence en fer peut conduire à des supplémentations inadaptées, parfois contre-productives, et à négliger d’autres causes : inflammation chronique, déséquilibres nutritionnels, pathologies infectieuses, etc.

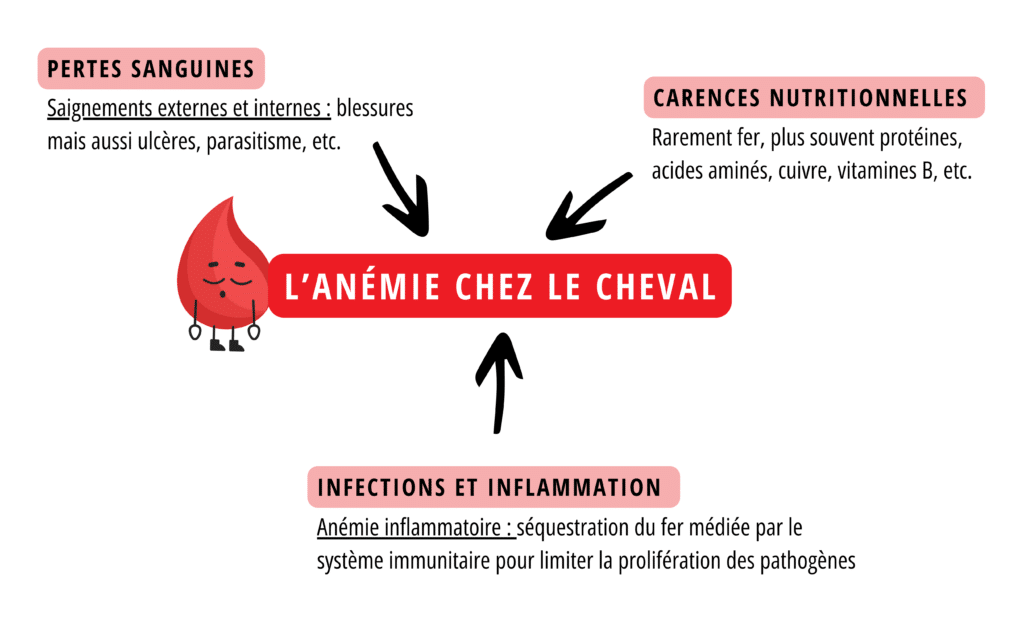
Première hypothèse : les pertes sanguines
L’anémie se définit par une diminution du nombre de globules rouges ou par une concentration d’hémoglobine inférieure à la normale. Lorsqu’elle survient chez le cheval, une hypothèse qui peut être explorée est celle d’une perte de sang, qu’elle soit interne ou externe.
En effet, toute hémorragie entraîne une diminution du volume sanguin total, réduisant le nombre de globules rouges et la quantité d’oxygène transportée dans l’organisme. Ces pertes sanguines peuvent résulter de traumatismes évidents, mais aussi de saignements internes plus discrets : ulcères gastriques, hémorragies pulmonaires à l’effort ou encore infestations parasitaires provoquant des pertes chroniques de faible intensité. Dans tous ces cas, l’anémie est bien réelle, mais elle ne découle pas d’un manque de fer alimentaire mais d’une diminution directe du volume de sang circulant.
Une autre cause importante d’anémie est la destruction accrue des globules rouges (hémolyse). Dans ce contexte, les globules rouges sont détruits plus rapidement qu’ils ne sont produits, ce qui entraîne une anémie dite hémolytique. Les origines de cette destruction peuvent être variées : réactions immunitaires, maladies auto-immunes, troubles hépatiques, exposition à certaines toxines végétales, ou encore infections par des bactéries, virus ou parasites capables d’endommager directement la membrane des globules rouges.
EXEMPLE CONCRET : LA PIROPLASMOSE

Cette maladie, provoquée par des protozoaires appelés piroplasmes, illustre parfaitement ce type d’anémie. Les parasites (Theileria equi et Babesia caballi) se développent à l’intérieur des globules rouges, les détruisant au fur et à mesure de leur cycle. Chaque fois qu’ils se multiplient, ils provoquent l’éclatement des hématies (hémolyse). Cette destruction massive des globules rouges entraîne une anémie parfois sévère, sans lien avec une carence en fer, mais directement liée à l’infection parasitaire. Ainsi, lors d’une piroplasmose, la prise de sang révèle une anémie, mais celle-ci traduit une atteinte infectieuse et hémolytique, et non un déficit en fer. Comprendre cette distinction est essentiel pour orienter le diagnostic et mettre en place un traitement adapté.
Récemment, l’IFCE a présenté des données issues du projet PiroGoTick. Selon ces résultats, environ 38% des chevaux en France seraient porteurs dits « asymptomatiques ». La piroplasmose constitue donc un véritable enjeu en médecine équine, notamment dans
l’approche diagnostique des anémies. Elle ne doit pas être envisagée uniquement sous l’angle des formes aiguës et cliniquement « évidentes », mais aussi dans ses expressions subcliniques, beaucoup plus fréquentes qu’on ne le pense.
Anémie inflammatoire : le fer est présent mais non disponible
Certaines anémies apparaissent dans un contexte d’inflammation chronique, lié à une infection persistante, à des troubles digestifs ou à une maladie métabolique. On parle alors d’anémie inflammatoire. Ce type d’anémie est particulier : le fer est bien présent dans l’organisme, mais il n’est plus disponible pour la fabrication des globules rouges.
Ce phénomène s’explique par un mécanisme naturel de défense appelé immunité nutritionnelle. Lorsqu’un agent pathogène envahit l’organisme, le système immunitaire cherche à le priver des nutriments essentiels à sa survie, notamment le fer, afin de limiter sa prolifération.
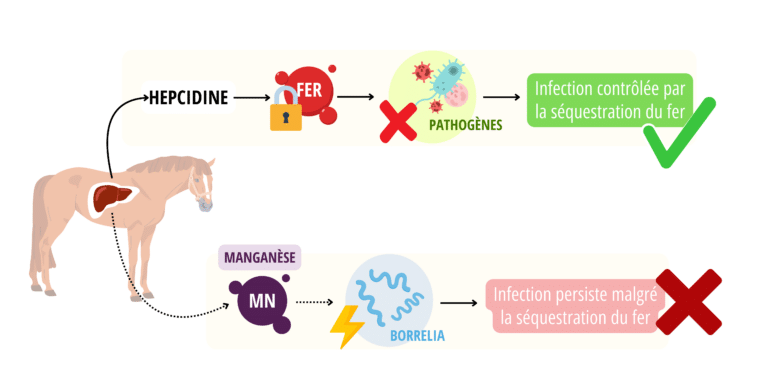
Sous l’effet de l’inflammation, le foie augmente la production d’une hormone clé : l’hepcidine. Véritable régulatrice du métabolisme du fer, elle se fixe sur les canaux de sortie du fer situés sur les cellules intestinales et les macrophages. Ce verrouillage bloque à la fois l’absorption du fer alimentaire et la libération du fer stocké dans les réserves.
Résultat : les analyses sanguines montrent un taux de fer sérique faible, mais les réserves corporelles (ferritine) restent normales ou parfois élevées. Le fer est donc présent, mais séquestré et inaccessible aux pathogènes comme aux cellules sanguines. Cette stratégie de défense protège le cheval : les pathogènes ne trouvent plus le fer dont ils ont besoin pour se multiplier. Ces mécanismes sont notamment utilisés par Escherichia coli, Rhodococcus equi et certaines infections virales.
Ces infections peuvent provoquer : fatigue, baisse de performance, muqueuses pâles – signes classiques d’anémie – mais la supplémentation en fer n’est pas efficace car le fer est séquestré volontairement par le métabolisme du cheval. Et la cause de l’anémie n’est, cette fois encore, pas un manque de fer. En ajouter demande donc à l’organisme d’en séquestrer encore plus, ce qui peut perturber la réponse immunitaire et, paradoxalement, favoriser le développement du pathogène !
Cas particulier : utilisation du manganèse par Borrelia b.
La bactérie responsable de la maladie de Lyme, ou Borréliose de Lyme, présente une particularité exceptionnelle dans le monde vivant : elle peut survivre et se multiplier sans avoir recours au fer. Alors que la plupart des organismes en dépendent pour fabriquer des protéines et des enzymes nécessaires à leur survie et à leur virulence, ce n’est pas le cas des Borrélies.
À la place, ces bactéries utilisent le manganèse pour constituer certaines de leurs enzymes essentielles. Ce remplacement leur procure un avantage évolutif majeur : lors d’une infection, l’organisme du cheval limite volontairement la disponibilité du fer dans le sang grâce à l’action de l’hepcidine, une hormone qui empêche son absorption et sa circulation. Ce mécanisme, qui peut provoquer une anémie passagère, vise à affamer les agents pathogènes dépendants du fer. Cependant, étant insensible à cette privation, les Borrélies continuent de se développer en exploitant le manganèse.
Cette adaptation unique leur permet d’échapper à une défense immunitaire pourtant très efficace contre la plupart des microbes. Elle contribue également à expliquer pourquoi la maladie de Lyme peut devenir chronique et reste parfois difficile à traiter, d’autant que la majorité des fourrages apportent des quantités de manganèse bien suffisantes à couvrir les besoins des chevaux.

Ce que la surcharge en fer chez d’autres espèces nous apprend
Des travaux sur la surcharge en fer chez le rhinocéros noir sous soins humains apportent des éléments intéressants pour la compréhension globale du métabolisme du fer.
Contrairement à l’hémochromatose humaine (accumulation excessive de fer dans l’organisme), souvent génétique, la surcharge observée chez le rhinocéros noir semble majoritairement liée à l’alimentation et à la biodisponibilité du fer. Les rhinocéros sauvages, qui gèrent eux-mêmes leur alimentation (feuilles, herbes sauvages, etc.), ne présentent pas de surcharge en fer, alors que ceux dont l’alimentation est gérée par l’humain (à base de fourrages récoltés et de luzerne notamment) finissent par en développer une. Chez le cheval, aucune pathologie génétique majeure du métabolisme du fer n’a été identifiée à ce jour.
Chez cette espèce, on observe une accumulation progressive de fer, associée à des lésions hépatiques et à divers troubles systémiques. Contrairement à l’hémochromatose humaine — une pathologie le plus souvent d’origine génétique caractérisée par une accumulation excessive de fer — la surcharge décrite chez le rhinocéros noir semble principalement liée à des facteurs nutritionnels, notamment à la composition de la ration et à la biodisponibilité du fer. Les rhinocéros vivant à l’état sauvage, capables de sélectionner eux-mêmes une alimentation diversifiée (feuillages, herbes naturelles, végétaux ligneux, etc.), ne présentent pas de surcharge en fer, contrairement aux individus maintenus en captivité, dont l’alimentation, gérée par l’humain, repose majoritairement sur des fourrages récoltés et des apports élevés de luzerne, et chez lesquels cette affection est fréquemment décrite. À ce jour, aucune affection génétique comparable affectant le métabolisme du fer n’a été mise en évidence chez le cheval, suggérant que les déséquilibres observés dans cette espèce relèvent davantage de facteurs environnementaux et nutritionnels que d’une prédisposition intrinsèque.
Ces travaux rappellent plusieurs points fondamentaux :
- Le fer est extrêmement régulé.
- Il n’existe quasiment pas de voie d’excrétion active du fer.
- L’équilibre repose principalement sur le contrôle de l’absorption intestinale par l’hepcidine.
- Une saturation excessive de la transferrine (>60% chez le rhinocéros) expose à la présence de fer circulant non lié, capable d’induire un stress oxydatif important.
Il est essentiel de préciser que le cheval n’est pas un rhinocéros. Les deux espèces partagent une fermentation du gros intestin, ce qui a justifié l’utilisation du cheval comme modèle expérimental dans certaines études de chélation du fer, mais leur métabolisme du fer n’est pas identique. Les données issues d’autres espèces doivent donc être interprétées avec prudence. Elles ne peuvent être transposées directement, mais elles permettent d’illustrer des mécanismes biologiques universels : rôle de l’hepcidine, saturation de la transferrine, stockage macrophagique, stress oxydatif induit par le fer libre.
Excès de fer : un risque théorique mais réel
Chez le cheval, les cas de toxicité du fer rapportés par les études scientifiques sont rares, mais l’absence actuelle de données robustes ne signifie cependant pas absence d’effet biologique. En pratique, certains professionnels et acteurs de terrain rapportent depuis longtemps des associations cliniques suggérant que le statut en fer pourrait influencer certains déséquilibres métaboliques. Ces observations ne remplacent pas des preuves expérimentales, mais elles invitent à la prudence : l’absence de consensus scientifique ne doit pas être interprétée comme une preuve d’innocuité.
Le lien entre fer, inflammation et métabolisme énergétique est un champ de recherche émergent en médecine comparée. Chez le cheval, ces interactions restent encore peu étudiées et il est peu probable que cette espèce soit celle pour laquelle nous disposerons des réponses les plus rapides ou les plus complètes.
Cependant, comme chez toutes les espèces, un excès de fer libre peut favoriser le stress oxydatif.
Anémie nutritionnelle : au-delà de la carence en fer
Protéines et acides aminés
Les globules rouges sont constitués de protéines et, en l’absence d’acides aminés essentiels, leur synthèse est compromise.
Chez les chevaux nourris avec des régimes riches en fourrages (ce qui devrait être le cas de tous, le fourrage à volonté étant la règle en l’absence de pathologies) le premier acide aminé limitant est la lysine, qu’il est donc nécessaire de compléter. Vient ensuite la méthionine, souvent déficiente chez les chevaux. Il est donc important d’apporter ces acides aminés essentiels afin d’éviter une anémie de production, due à une fabrication insuffisante de globules rouges.
Cuivre
Le cuivre joue un rôle clé dans la mobilisation du fer et dans la synthèse de l’hémoglobine, ce qui le rend indispensable à la formation des globules rouges. Le cuivre contribue également à protéger les globules rouges contre le stress oxydatif, limitant ainsi leur destruction prématurée.
Une carence en cuivre peut donc provoquer une anémie fonctionnelle même si le fer total de l’organisme est suffisant. Ce type d’anémie peut parfois être confondu avec une anémie ferriprive (par manque de fer), conduisant à une supplémentation en fer. Or, un excès de fer peut inhiber l’absorption du cuivre (et du zinc), aggravant la carence en cuivre et créant un cercle vicieux : la supplémentation en fer, pensée pour corriger l’anémie, amplifie en réalité l’anémie par carence en cuivre. Cette situation est particulièrement fréquente lorsque les apports en fer sont élevés et que le cheval n’est pas correctement supplémenté en cuivre.
L’herbe et le foin apportent en moyenne 4mg de cuivre par kg de matière sèche (MS). Les besoins minimums d’un cheval de 500kg à l’entretien sont d’environ 150mg de cuivre par jour. Pour atteindre cette quantité uniquement grâce au foin ou à l’herbe, le cheval devrait consommer 25 kg de MS par jour. Or, l’ingestion volontaire se situe généralement autour de 2 à 2,5% du poids corporel, soit environ 10 à 12kg de MS par jour pour un cheval de 500kg (soit entre 40 et 48mg de cuivre ingérés). On est donc bien en-dessous des besoins nécessaires, ce qui rend la complémentation en cuivre indispensable.
L’absorption du cuivre peut être réduite en cas d’excès de fer ou de zinc. Le zinc, relativement peu présent dans les fourrages (environ 22 mg par kg de matière sèche), nécessite souvent une complémentation pour maintenir un équilibre optimal. Idéalement, le ratio fer : cuivre : zinc : manganèse dans la ration devrait se situer entre 4:1:3:3 et 10:1:3:3 (soit entre 4 et 10 fois plus de fer que de cuivre, et 3 fois plus de zinc et de manganèse que de cuivre). Dans un foin classique, ce ratio est plutôt autour de 50:1:5:29, ce qui représente un excès important de fer et de manganèse par rapport au cuivre. Il est donc nécessaire d’apporter du cuivre supplémentaire afin de rééquilibrer ces ratios et garantir une absorption et une utilisation optimale de tous les minéraux, tout en limitant les apports supplémentaires en fer et en manganèse.
Vitamines B
Les vitamines B, en particulier la B9 et la B12, jouent un rôle essentiel dans la production de globules rouges. Une carence entraîne une anémie mégaloblastique, caractérisée par des globules rouges de taille anormalement grande et inefficaces.
Chez le cheval, l’état de la flore digestive est déterminant pour la disponibilité de ces vitamines, car elles sont en partie synthétisées par les micro-organismes qui la composent. Or, cette flore est très sensible à de nombreux stress : maladies, changements d’environnement, transports, activité physique intense, etc., autant de situations qui peuvent altérer sa capacité à produire ces vitamines.
Dans ces conditions, il est donc recommandé de complémenter le cheval en vitamines B pendant les périodes à risque afin de prévenir l’apparition d’une anémie liée à leur déficit, et de toujours veiller à soutenir la flore.
Cas particuliers : le manque de fourrage ou le fourrage très pauvre en fer

Le besoin en fer d’un cheval de 500kg est de 400mg par jour. En moyenne, le fourrage apporte 200mg de fer par kilo (avec une fourchette pouvant varier de 40mg à plus de 2000mg par kilo).
En consommant 2 à 2,5% de son poids en MS de fourrage, le cheval va consommer environ 2000mg de fer (400mg au minimum, parfois plus de 20 000mg).
À moins de manquer drastiquement de fourrage (chevaux dénutris), il est donc peu probable (pour ne pas dire impossible) que notre cheval manque de fer. L’organisme ayant la capacité de stocker le fer, si l’on se retrouve dans le rare cas où le fourrage est pauvre en fer (ce qui ne veut pas dire qu’il le restera d’une année à l’autre en étant fait sur la même parcelle), alors l’organisme pourra le déstocker, ce qui sera bienvenu (les foies de chevaux autopsiés étant souvent noirs en raison de l’excès de fer accumulé).

Quid de l’assimilation du fer ?
Il est souvent avancé que le fer des végétaux est moins biodisponible que le fer d’origine animale. Il faut noter 2 choses importantes à ce sujet :
- Cette distinction repose essentiellement sur des travaux conduits chez l’humain, dont l’alimentation associe fer héminique et fer non héminique. Le cheval, en revanche, est un herbivore strict dont l’alimentation naturelle apporte presque exclusivement du fer non héminique, présent dans les végétaux majoritairement sous forme ferrique (Fe³⁺). Les extrapolations consistant à appliquer au cheval des valeurs d’assimilabilité du fer établies chez des espèces omnivores doivent donc être interprétées avec prudence, compte tenu des différences majeures de physiologie digestive et d’exposition alimentaire.
- Les recommandations nutritionnelles établies pour le cheval ont été déterminées à partir de régimes conventionnels à base de fourrages et intègrent implicitement une biodisponibilité moyenne du fer alimentaire. Se fonder sur une assimilation supposée limitée pour justifier des apports largement supérieurs aux besoins pose alors question. Appliqué à d’autres oligo-éléments essentiels, tels que le sélénium ou le cuivre, ce raisonnement pourrait conduire à accepter des excès potentiellement toxiques.

LE MOT DU véto
Si une anémie est détectée à la prise de sang, nous conseillons de chercher la cause avant tout :
- Prises de sang complémentaires pour rechercher des maladies vectorielles (Lyme, anaplasmose, leptospirose, piroplasmose) ou des marqueurs inflammatoires.
- Analyses des antécédents du cheval, de son suivi vermifuge, etc. pour identifier de possibles pertes sanguines.
- Vérifier si sa ration couvre ses besoins (éventuellement via une analyse de fourrage en complément).
- Etc.
Les supplémentations en fer peuvent donner le sentiment de « soigner » l’anémie lorsque l’on fait un contrôle sanguin rapproché, mais il s’agit en général d’une amélioration à court terme. L’objectif étant de soigner un cheval et non pas une prise de sang, aller à la cause (même si cela nécessite plus d’investigations) montre de meilleurs résultats à long terme.
Docteur vétérinaire Florence.F
En conclusion, l’anémie chez le cheval est rarement (pour ne pas dire jamais – sauf cas bien particuliers) synonyme de carence en fer.
Elle peut résulter de pertes sanguines, de destruction accrue des globules rouges, d’inflammations ou de déficits en nutriments essentiels comme le cuivre, certains acides aminés et les vitamines B. Comprendre les causes réelles est crucial car un diagnostic précis permet d’adapter la prise en charge et d’éviter des supplémentations inutiles ou contre-productives.
De plus, la régulation étroite de l’absorption intestinale du fer chez le cheval ne doit pas être interprétée comme la garantie d’une tolérance illimitée aux apports excessifs. Ce contrôle physiologique vise précisément à limiter l’entrée du fer lorsque celui-ci est disponible en quantité suffisante. Il constitue ainsi un mécanisme de protection contre l’accumulation excessive plutôt qu’un argument justifiant de dépasser largement les besoins établis.
Bibliographie :
- Aguirre, J. D., Clark, H. M., McIlvin, M., Vazquez, C., Palmere, S. L., Grab, D. J., Seshu, J., Hart, P. J., Saito, M., & Culotta, V. C. (2013). A manganese-rich environment supports superoxide dismutase activity in a Lyme disease pathogen, Borrelia burgdorferi. Journal of Biological Chemistry, 288(12), 8468–8478. https://doi.org/10.1074/jbc.M112.433540
- Ganz, T. (2009). Iron in innate immunity: Starve the invaders. Current Opinion in Immunology, 21(1), 63–67. https://doi.org/10.1016/j.coi.2009.01.011
- Geor, R. J., Harris, P. A., & Coenen, M. (2013). Equine applied and clinical nutrition: Health, welfare and performance. Saunders/Elsevier. ISBN 978-0-7020-3422-0
- Kulik-Rechberger, B., & Dubel, M. (2024). Iron deficiency, iron deficiency anaemia and anaemia of inflammation – An overview. Annals of Agricultural and Environmental Medicine, 31(1), 151–157. https://pubmed.ncbi.nlm.nih.gov/38549491/
- National Research Council. (2007). Nutrient Requirements of Horses: Sixth Revised Edition. The National Academies Press. https://doi.org/10.17226/11653
- Ni, S., Yuan, Y., Kuang, Y., & Li, X. (2022). Iron metabolism and immune regulation. Frontiers in Immunology, 13, 816282. https://doi.org/10.3389/fimmu.2022.816282
- Osterholm, E. A., & Georgieff, M. K. (2015). Chronic inflammation and iron metabolism. Journal of Pediatrics, 166, 1351–1357.e1. https://doi.org/10.1016/j.jpeds.2015.01.017
- Sullivan, K. (2025). Mitigating Iron Overload Disorder in the Black Rhino: Comparative solutions to a cross-species issue. Communication présentée à la No Laminitis Conference (ECIR 2025).
- Troxell, B., Xu, H., & Yang, X. F. (2012). Borrelia burgdorferi, a pathogen that lacks iron, encodes manganese-dependent superoxide dismutase essential for resistance to streptonigrin. Journal of Biological Chemistry, 287(23), 19284–19293. https://doi.org/10.1074/jbc.M112.344903




